약평위 1차 심의서 급여적정성 없다고 결론...30일 내 이의신청 가능
오리지널 임상적 유용성 없으면 제네릭 비교 임상 의미없어

위염치료에 사용하는 생약제제 '애엽추출물(대표품목 스티렌)' 성분 의약품이 급여적정성이 없는 것으로 심의되면서 동등성 재평가 진행 여부에 관심이 쏠린다.
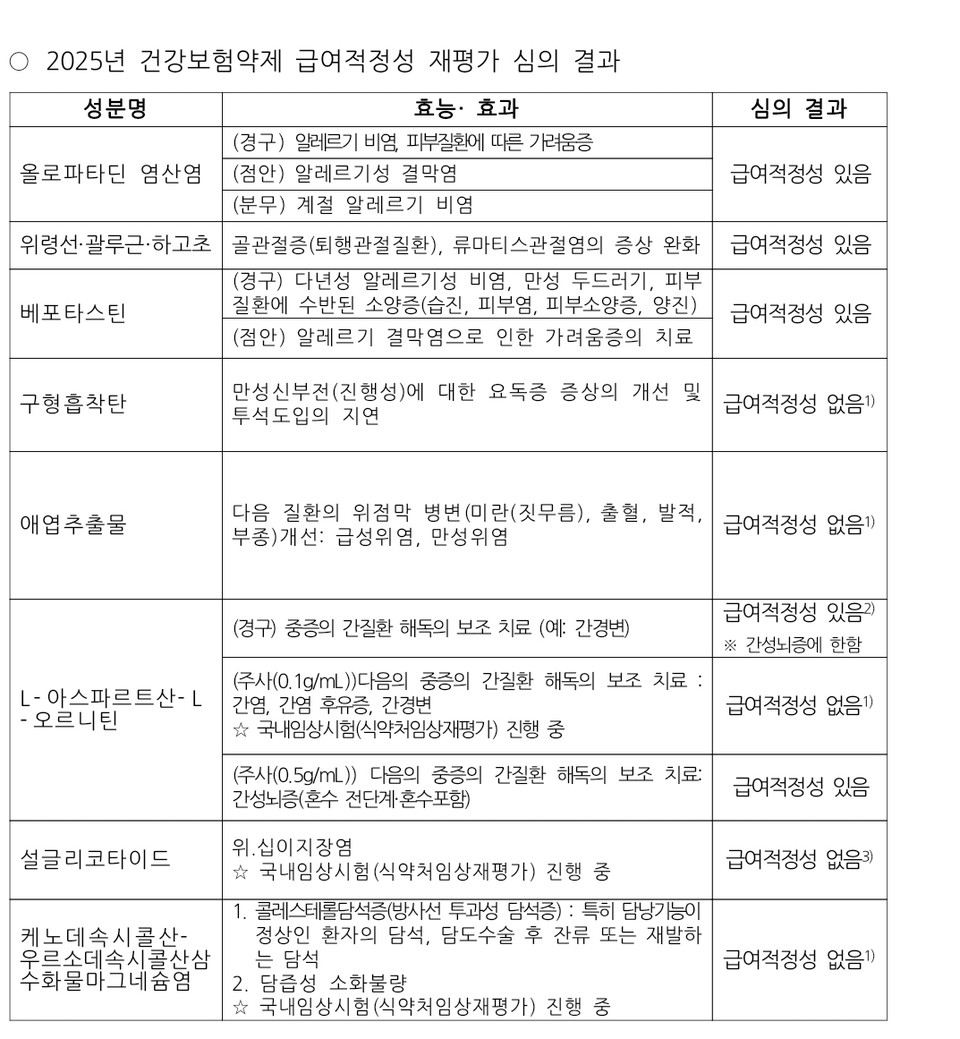
건강보험심사평가원은 지난 7일 약제급여평가위원회 심의 결과 애엽추출물이 '급성위염과 만성위염의 위점막 병변, 출혈, 발적 개선'에 급여적정성이 없는 것으로 결론이 나왔다고 밝혔다. 특히, 해당 의약품은 임상적 유용성 근거가 없다고 부연했다.
이는 1차 심의 결과로 해당 성분을 가진 제약사들은 이의신청할 수 있으며 심평원은 추가 자료를 검토 후 약평위에 재상정해 2차 심의를 통해 급여적정성을 결정한다.
현재 애엽추출물 오리지널 약제 '스티렌'을 보유한 동아에스티 등은 이의신청을 진행할 것으로 보인다.
여기에 제약사들의 이목이 집중되는 또다른 이유는 애엽추출물의 급여적정성 인정 여부가 식품의약품안전처가 진행 중이 동등성 재평가와도 연관되기 때문이다.
심평원과는 별개로 식약처는 올해 생약제제 동등성 재평가를 진행 중으로, 여기에는 애엽추출물이 포함됐다. 애엽추출물 제제는 전체 재평가 품목의 약 64%인 135 품목을 차지하고 있다.
당초 제약사들은 생약제제의 경우 생약(주로 식물)의 추출물 그 자체를 하나의 주성분으로 관리하고 있으며 다양한 성분이 함유돼 명확하게 규명하기 어렵기 때문에 생동시험을 할수 없다고 주장했었다.
하지만 식약처는 생약제제 전문약 동등성 재평가를 실시해야한다는 입장으로, 불참을 결정한 제약사들을 제외하고는 지난 6월 비교임상 계획서를 제출한 상황이다.
다만 동등성 재평가는 오리지널인 대조약과 비교해 효과를 입증해야 하기 때문에 '스티렌'과 대원제약 '오티렌'은 대상이 아니다. 여기서 오리지널인 스티렌이 임상적 유용성 근거가 없다고 최종 결론이 나면 비교 임상은 의미가 없게 된다.
즉, 스티렌 제네릭들은 오리지널과 비교 임상을 진행 중이지만 동등성 재평가이기 때문에 '스트렙토키나제'나 '콜린알포세레이트'의 임상재평가 케이스와는 다르다.
비용효과성을 따져 약가를 인하하는 케이스도 있지만 이의신청 시 추가 자료를 통해 임상적 유용성을 어느 정도 입증하는지 따져봐야 할 것으로 보인다.
심평원 측은 "급여적정성 재평가 심의 결과를 통보받은 후 30일 이내 이의신청서를 제출할 수 있으며 제출된 내용은 약평위 재심의를 거치게 될 것"이라고 말했다.
