FDA·EMA 등 신규접근법(NAMs) 도입 가속화...동물실험 종식 선언
미국이 동물실험 중심 연구에 대한 자금 지원을 종료하고 신규접근법(NAMs)을 의무화하면서 제약바이오산업도 패러다임 전환을 예고했다.
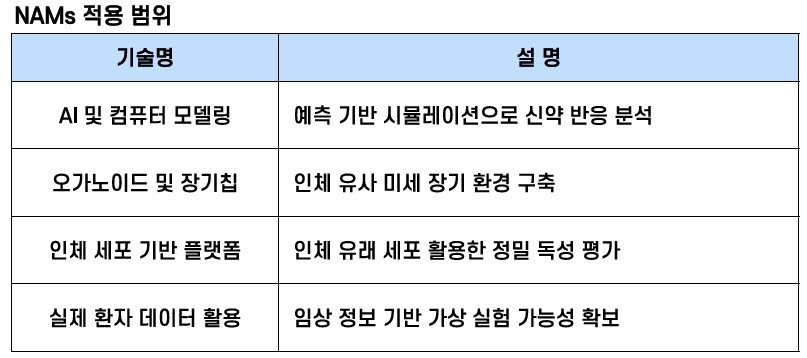
신규접근법(NAMs, New Approach Methologies)은 기존 동물실험을 대체하거나 보완하기 위해 개발된 비(非)동물 기반 시험·평가 방법으로 △인체유래세포를 활용한 정밀 독성 평가 △인체 장기 기능을 모사한 오가노이드·장기칩 △인공지능(AI) 및 컴퓨터 모델링을 활용한 예측 기반 시뮬레이션 △임상정보 기반 환자 데이터 분석 등을 포함한다.
10일 한국바이오의약품협회 정책브리프에 따르면 미국 국립보건원(NIH, National Institute of Health)은 최근 동물실험 모델만 사용하는 연구 지원을 공식적으로 종료하고, NAMs로 전환한다는 방침을 공식 발표했다.

이같은 결정에는 그동안 신약 임상에서 동물실험이 실효성 입증에 한계를 드러낸 점도 영향을 미친 것으로 보인다. 바이오의약품협회는 리포트에서 "동물실험을 통과한 약물의 90% 이상이 실제 임상에서 안전성 또는 유효성 부족으로 FDA 승인을 받지 못한다"고 언급한 FDA 자문위원의 발언에 주목했다.
미국은 신약개발을 포함한 첨단 분야에서 동물실험을 배제한 연구를 촉진하기 위해 관련 조직을 강화하는 등 속도를 내고 있다.
NIH는 국장 산하 조직으로 연구혁신·검증·적용청(ORIVA, Office of Rearch Innovation, Verification and Application)을 신설해 NAMs 기술 개발과 검증 및 확산을 추진할 계획이다.
ORIVA는 앞으로 △NAMs 기반 연구 지원 △심사기준 정비 △관계기관 협력체계 구축 △연례보고서 발간 등을 통한 동물대체 기술 제도화를 전담하게 되며, 전면 전환보다는 점진적 이행을 통해 안착을 시도할 가능성이 제기된다.
유럽연합(EU)도 안전성 평가 영역에서 동물 사용을 축소하기 위한 로드맵을 수립 중이며, 유럽의약품청(EMA) 주도로 NAMs 적용을 가이드라인 검토에 착수했다.
이같은 정책 전환은 글로벌 제약바이오가업과 임상시험수탁기관(CRO)를 포함한 관련 산업의 비즈니스모델에 직접적인 영향을 줄 것으로 예상됨에 따라 국내 제약바이오산업도 발빠른 대응이 요구된다. 신약개발 과정에 NAMs 기반 첨단기술이 도입되면 예측 정밀도가 높아지고 R&D 비용이 절감될 것으로 기대된다.
바이오의약품협회는 "미국, 유럽 등 각국이 NAMs 전환을 가속화함에 따라 국내 제약바이오산업도 관련 기술 도입과 규제 대응 시스템 구축, 국제협력 활성화를 통해 환경 변화에 대비해야 한다"며 "동물실험 중심 인프라를 바꾸고 글로벌 수준의 기술을 개발해 새로운 시장을 확보해야 한다"고 분석했다.
이를 위해 "NAMs 기반 기술 개발에 대한 정부 차원의 적극적 지원이 필요하다"며 "NAMs 가이드라인을 조기 수립하고 산학 협력을 통해 기술 개발과 인력 양성을 추진해야 한다"고 제언했다 .
협회는 이어 "구조적 전환 필요성에 대한 산업계 공감대를 형성하는 등 업계 차원의 노력도 필요하다"며 "초기 투자 부담에 대한 정부 지원을 요청하고 새로운 글로벌 규제환경을 모니터링해 적응력을 확보해야 한다"고 강조했다.
